Eccoci ed entriamo subito nel vivo cercando di capire quali siano i principali fattori in grado di influenzare la velocità delle reazioni enzimatiche. Ne vedremo tre tra quelli che riteniamo essere i più importanti in ambito alimentare: temperatura, pH e attività dell’acqua (aw).

Temperatura: un fattore molto importante che può influenzare in maniera decisiva l’andamento e la velocità di una reazione enzimatica. L’equazione di Arrhenius (sopra) mette in relazione la costante della velocità di reazione con la variazione della temperatura e, nella pratica, ci dice che entro certi limiti la velocità di una reazione raddoppia all’aumentare di ogni 10 °C. In ambito enzimatico, come regola generale, valori intorno ai 30–45 °C sono considerati l’optimum anche se specifici enzimi in uso nell’industria alimentare possono avere valori ottimali intorno ai 75–85 °C. Oltre una certa temperatura si ha la denaturazione termica con perdita di ogni attività enzimatica. Conoscendo questa caratteristica, sia nella pratica culinaria che in quella industriale, è uso effettuare un “blanching” (scottatura) anche per inattivare gli enzimi presenti negli alimenti stessi che potrebbero originare reazioni secondarie non volute o per migliorarne qualche caratteristica. E’ il caso di alcune tipologie di frutta che vengono poste per qualche secondo in acqua bollente per mantenerne poi il colore brillante.
Una curiosità: anche se può sembrare strano, il congelamento, in certi casi, porta ad aumentare il numero delle reazioni enzimatiche così come la velocità delle stesse rispetto a quanto ci si aspetterebbe. Questo fenomeno può essere spiegato, se pur il maniera semplificata, con l’effetto concentrazione (del quale abbiamo dato cenno qui) e il conseguente maggior contatto tra enzimi e substrati.
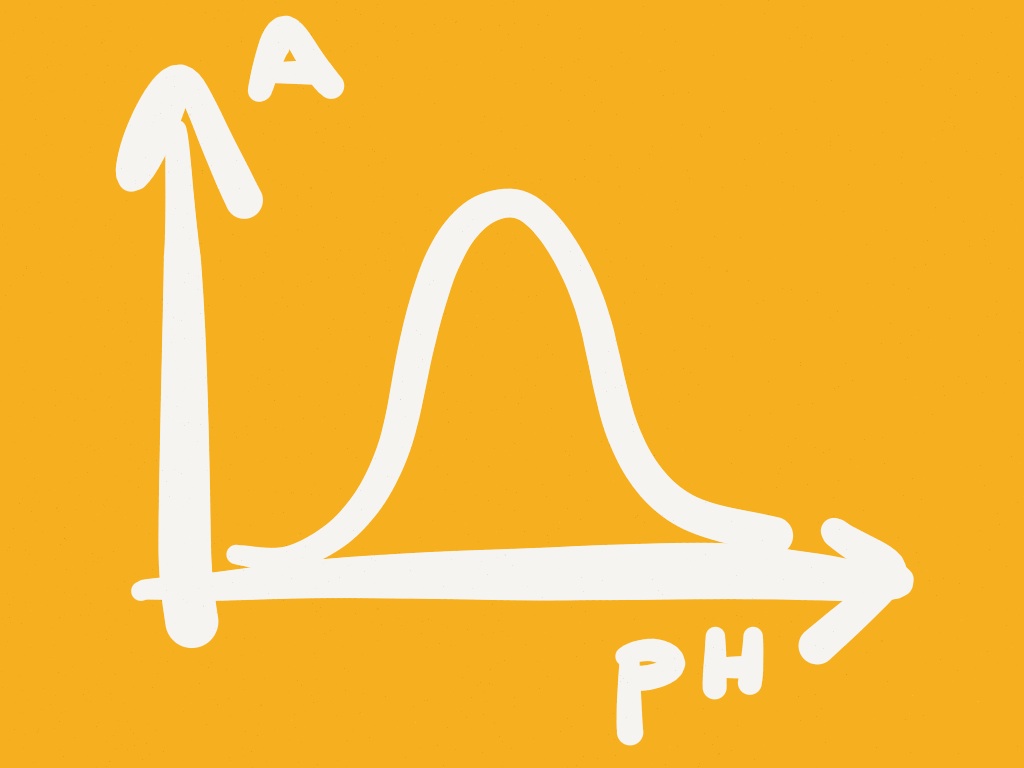
pH: ogni enzima ha un suo valore optimum di attività e questo, negli alimenti, in genere si avvicina a valori neutri o vicino alla neutralità. Conoscendo questa caratteristica si spiega anche perché, per inibire l’imbrunimento, si immergano le mele in una soluzione di acqua e limone una volta tagliate. L’acidificazione rallenta e/o inibisce gli enzimi e le reazioni capaci di dare questo indesiderato fenomeno tipico anche dei frutti “ammaccati”.
Attività dell’acqua (aw): l’acqua è il mezzo nel quale praticamente qualsiasi reazione enzimatica avviene. E’ necessario però che questo solvente naturale si presenti in forma libera affinché un enzima riesca ad agire. Se un alimento presenta una percentuale di acqua al di sotto di un certo limite, l’enzima è inattivo. Processi quali la disidratazione osmotica, la liofilizzazione e l’essiccazione possono ad esempio, abbassando il valore dell’attività dell’acqua di un prodotto alimentare, “bloccare” le attività enzimatiche e preservare le caratteristiche qualitative volute.

Certamente altri elementi possono influenzare le reazioni enzimatiche, soprattutto quando si parla di inibirle. L’utilizzo di additivi specifici è notoriamente fatto per evitare l’imbrunimento di alcuni vegetali (a tale fine si usa spesso l’anidride solforosa, SO2). Alcune tecnologie di produzione, diversi metodi di conservazione, molti packaging ed altri fattori ancora possono essere impiegati per eliminare e/o rallentare talune reazioni enzimatiche. In pratica, non esiste una sola via di azione così come non esistono enzimi buoni ed enzimi cattivi. Ricordiamo a tal proposito che alcune reazioni enzimatiche sono volutamente innescate, favorite o lasciate procedere perchè in grado di conferire positive e peculiari caratteristiche ad alcuni alimenti (vedi la fermentazione di tè, caffè e cioccolato, la burrificazione, la vinificazione, ecc…).
Continuiamo a studiare e ad indagare su nuove applicazioni e soluzioni che portino ad un generale e reale miglioramento sia nei processi che nei prodotti.
Let’s food together!